REAKSI POLISIKLIK DAN REAKSI PERISIKLIK
SENYAWA POLISIKLIK
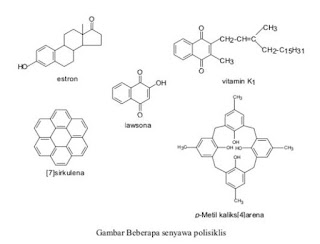
Senyawa polisiklik yaitu senyawa yang terbentuk dari dua bahkan lebih dari dua sistem cincin (siklik). Banyak sekali senyawa polisiklik yang berasal dari bahan alam maupun berasal dari hasil sintesis. Senyawa polisiklik yang berasal dari bahan alam yaitu estron : hormon yang terdapat pada wanita, Lawson : zat warna kuning yang dihasilkan dari tanaman tropis lawsonia inermis ataupun vitamin k. Sedangkan, senyawa polisiklik yang berasal dari hasil sintesis. Ex: kaliks(4)arena serta sirkulena.
Contoh lain dari senyawa polisiklik yaitu grafit yang strukturnya terbentuk dari bidang cincin benzena terpadu. Grafit memiliki sifat yang licin yang diakibatkan dari bidang yang mampu bergerak satu dengan yang lainnya. Dari sifatnya ini, grafit sering dipakai untuk pelumas. Karena elektron n nya yang bisa berpindah ataupun terdelokalisasi , maka grafit ini bisa menghantarkan arus listrik serta yang dipakai pada elektroda pada baterai.
Senyawa polisiklik dibagi dalam beberapa jenis, yang pertama pembagian senyawa polisiklik berdasarkan sifat aromatisnya :
- Senyawa polisiklik aromatis : senyawa yang memiliki sifat aromatis, seperti memiliki struktur cincin datar, berhibridisasi sp 2, serta mengikuti aturan Huckel. Contohnya naftalen.
- Senyawa polisiklik non aromatis : senyawa yang tidak memiliki sifat aromatis. Contohnya bisiklo[4,4,0]dekena.
Kedua berdasarkan jenis atom yang menyusun cincinnya :
- Homosiklik (korbonsiklik)
- Heterosiklik
Ketiga berdasarkan cara penggabungan cincinnya :
- Terpadu : ada orto, berjembatan, serta spiro.
- Tepisah : ada jembatan tidak beranggota dan jembatan beranggota.
Kereaktifan Senyawa Polisikik Aromatik
Pada kereaktifan senyawa polisiklik aromatik terdapat 3 reaksi yaitu, reaksi oksidasi, reaksi reduksi dan reaksi substitusi. Senyawa polisiklik aromatik lebih reaktif daripada senyawa benzena terhadap reaksi reduksi, oksidasi serta substitusi. Kereaktifan ini dikarenakan bisa bereaksi dengan suatu cincin, sedangkan cincin yang lainnya dipertahankan.
REAKSI PERISIKLIK
Reaksi perisiklik yaitu suatu reaksi poliena yang terkonjugasi bisa berlangsung dengan mekanisme bersamaan, yaitu reaksi SN2 pada ikatan lama terlepas ketika ikatan baru terbentuk serta semuanya berlangsung dalam 1 tahap. Karakteristik suatu reaksi perisiklik adalah keadaan transisi siklik yang terlibat dengan ikatan phi nya. Ada 3 macam reaksi perisiklik diantaranya yaitu ;
- Reaksi Sikloadisi : pada dua molekul yang bersatu dan membentuk suatu cincin. Dimana dua ikatan phi dalam reaksi diubah menjadi ikatan sigma.Pereaksi yang terdapat pada reaksi Diels-Alder dikelompokkan menjadi diena dan dienofil. Pada reaksi ini tidak terjadi secara langsung melalui zat antara yang bersifat ion, tetapi diena serta dienofilnya yang mempengaruhi laju reaksinya. Contoh yang terjadi pada reaksi Diels-Alder. Sikloadisi dibagi menjadi beberapa jenis diantaranya : [2+2], [4+2], [4+4], [6+2]. [6+4], dan lain sebagainya. Dua angka yang terdapat menunjukkan bahwa jumlah elektron phi terlibat dalam suatu reaksi sikloadisi. Pada sikloadisi [2+2] bisa terjadi jika dalam reaksinya terdapat cahaya atau sinar uv dan dengan panjang gelombang yang sesuai, tetapi jika reaksi ini dipanaskan malah tidak mudah terjadi. Sedangkan pada sikloadisi [4+2] harus menggunakan panas tetapi bukan cahaya ultraviolet.
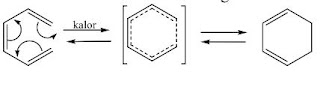
- Reaksi Elektrosiklik : merupakan suatu reaksi reversible dalam suatu senyawanya yang memiliki ikatan rangkap yang terkonjugasi menjadi siklisasi. Di dalam siklisasi ini phi yang memiliki 2 elektron digunakan sebgai pmbentuk ikatan sigma.
- Penataan Ulang Sigma-Tropik : penataan ulang pada molekul bersama-sama terjadi pada suatu atom ataupun gugus asam yang berpidah dari posisi 1 ke posisi yang lainnya.
PERMASALAHAN
1. Bagaimanakah kegunaan cahaya pada reaksi siklokadisi [2+2] dan panas pada reaksi siklokadisi [4+2]?
2. Bagaimanakah kegunaan dari senyawa polisiklik bagi kehidupan sehari-hari?
3. Mengapa senyawa polisiklik lebih reaktif daripada senyawa benzena terhadap reaksi oksidasi, reduksi, dan substitusi?





Saya Angesti Dhitya dengan NIM A1C117004 akan menjawab permasalahan ketiga dari riska. Mengapa senyawa polisiklik lebih reaktif daripada senyawa benzena terhadap reaksi oksidasi, reduksi dan substitusi. Saya akan mencontohkan naftalena. Naftalena lebih mudah mengalami reaksi tersebut karena naftalena cincin aromatiknua dapat dipecah dengan energi sebesar 25kkal/mol, sedangkan benzena membutuhkan energi sebesar 36kkal/mol untuk memecah 1 cincin aromatiknya.
BalasHapusKomentar ini telah dihapus oleh administrator blog.
BalasHapusSaya ulin ayu wulandari (A1C117024) akan coba menjawab permasalahan no 2. Contoh dari senyawa polisiklik diantaranya grafit. Grafit mempunyai sifat licin sehingga menyebabkan kemampuan bidang-bidang dapat bergeser satu sama lain. Berdasarkan sifat ini maka grafit sering digunakan sebagai pelumas. Akibat elektron π yang dapat berpindah-pindah dan terdelokalisasi, grafit dapat menghantarkan arus listrik dan digunakan sebagai elektrode pada baterai.
BalasHapusContohbberikutnya yaitu Naftalena digunakan sebagai pengusir ngengat, serta turunannya digunakan dalam bahan bakar motor dan pelumas. Aromatik polisiklik digunakan secara luas sebagai zat antara pada sintesis organik, misalnya dalam pembuatan zat warna (lihat kegunaan senyawa benzena pada pembahasan sebelumnya).
Saya Ariyansyah
BalasHapusNIM A1C117050
Saya akan mencoba membantu permasalahan no 1
Nomor satu untuk pelepasan ikatan phi dan membentuk senyawa siklik baru, makanya pasa reaksi sikloadisi diperlukan bantuan dari luar berupa cahaya dan panas.