KEKUATAN ASAM DAN BASA DALAM KIMIA ORGANIK
Asam Organik ialah suatu senyawa yang terdapat gugus karboksil, istilah ini diambil dari karbonil dan hidroksil. Suatu gugus yang berkaitan dengan gugus karboksil pada asam karboksilat dapat gugus apa saja, bahkan dapat gugus karboksil lainnya.
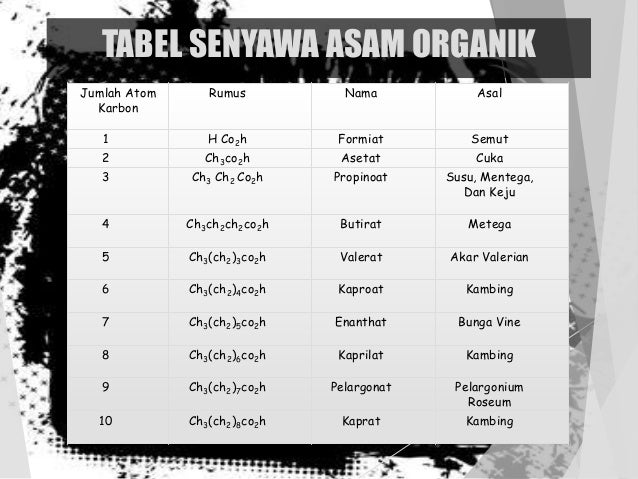
Asam Organik
Asam organik dicirikan oleh adanya atom hidrogen yang terpolarisasi positif. Terdapat dua macam asam organik, yang pertama adanya atom hidrogen yang terikat dengan atom oksigen, seperti pada metil alkohol dan asam asetat. Kedua, adanya atom hidrogen yang terikat pada atom karbon di mana atom karbon tersebut berikatan langsung dengan gugus karbonil (C=O), seperti pada aseton.
Metil alkohol mengandung ikatan O-H dan karenanya bersifat asam lemah, asam asetat juga memiliki ikatan O-H yang bersifat asam lebih kuat. Asam asetat bersifat asam yang lebih kuat dari metil alkohol karena basa konjugat yang terbentuk dapat distabilkan melalui resonansi, sedangkan basa konjugat dari metil alkohol hanya distabilkan oleh keelektronegativitasan dari atom oksigen.
Senyawa yang disebut dengan asam karboksilat, memiliki gugus –COOH, terdapat sangat banyak di dalam organisme hidup dan terlibat dalam jalur-jalur reaksi metabolik. Asam asetat, asam piruvat, dan asam sitrat adalah contohnya. Perlu dicatat bahwa pH fisiologis adalah sekitar 7.3, sehingga asam karboksilat sebagian besar terdapat sebagai anionnya, yaitu anion karboksilat, -COO-.
Basa Organik
Basa organik dicirikan dengan adanya atom dengan pasangan elektron bebas yang dapat mengikat proton. Senyawa-senyawa yang mengandung atom nitrogen adalah salah satu contoh basa organik, tetapi senyawa yang mengandung oksigen dapat pula bertindak sebagai basa ketika direaksikan dengan asam yang cukup kuat. Perlu dicatat bahwa senyawa yang mengandung atom oksigen dapat bertindak sebagai asam maupun basa, tergantung lingkungannya. Misalnya aseton dan metil alkohol dapat bertindak sebagai asam ketika menyumbangkan proton, tetapi sebagai basa ketika atom oksigennya menerima proton.
MANFAAT DAN KEGUNAAN ASAM ORGANIK
1. ASAM FORMIAT (Asam Semut/Asam Metanoat)
Asam formiat berwujud zat cair yang tak berwarna, mudah larut dalam air serta berbau tajam. Bila dalam jumlah sedikit ia terdapat didalam keringat, maka dari itu keringat biasanya berbau asam. Asam ini dapat menyebabkan lecet atau lepuh pada kulit bila terkena. Sifat yang khusus yang dimiliki asam formiat ialah dapat mereduksi, karena memiliki gugus aldehid. Kegunaan dari asam formiat ialah untuk mengumpulkan lateks, penyamakan kulit, serta pada proses pencelupan tekstil.
2. ASAM ASETAT (Asam Cuka/Asam Etanoat)
Asam asetat memilki kesaam sifat dengan asam formiat yaitu berwujud cair, tidak berwarna, mudah larut dalam air, serta berbau tajam. Larutan cuka sebagai makanan yang umum digunakan sehari-hari memiliki kadar 25% volume asam asetat, sedangkan asam asetat murni disebut asam asetat glasial digunakan untuk membuat selulosa asetat dalam industri rayon.
3. ASAM SITRAT
Asam sitrat juga terdapat dalam jeruk, yang dapat digunakan sebagai pengawet buah dalam kaleng.
4. ASAM STEARAT
Asam ini berbentuk padat, berwarna putih. Dalam kehidupan sehari-hari biasanya digunakan untuk pembuatan lilin.
Istilah "kuat" dan "lemah" dalam konteks ini tidak berhubungan dengan seberapa korosif atau kerasnya zat tersebut, tetapi hanya kemampuannya untuk terionisasi dalam air. Kemampuan suatu zat untuk makan melalui bahan lain atau merusak kulit lebih merupakan fungsi dari sifat-sifat asam itu, serta konsentrasinya. Meskipun, asam kuat lebih berbahaya secara langsung pada konsentrasi yang lebih rendah, asam kuat tidak lebih berbahaya daripada asam lemah.
Berikut tabel grafik kekuatan asam dan basa :

PERMASALAHAN
1. Mengapa pada metil alkohol diatas anionnya distabilkan dengan elektronegativitasi atom oksigen sedangkan asam asetat yang anionnya distabilkan melalui resonansi, Jelaskan!
asam sulfonat asam alkanoat
asam sulfonat asam alkanoat


2. Dilihat dari gugusnya mengapa asam sulfonat memiliki derajat keasaman yang lebih kuat dibandingkan dengan asam alkanoat, Jelaskan!

3. Coba Anda lihat senyawa ammonia dan metilamin yang hanya memiliki perbedaan cabang CH3 yang terdapat pada struktur metilamin. Bila dilihat dari struktur dan pKb pada gambar diatas manakah yang memiliki sifat basa yang lebih kuat, Jelaskan!


Halo riska!
BalasHapusBaiklah saya akan menjawab permasalahan no.2, menurut saya yang membuat asam sulfonat lebih asam dari asam alkanoat adalah karena polaritas nya yang berbeda. Dimana asam sulfonat lebih polar di banding kan alkanoat
halo riska,
BalasHapussaya akan menjawab permasalahan no. 3, menurut saya sifat basa yang lebih kuat ditunjukkan pada phenylamine. hal itu disebabkan pada struktur tersebut memiliki pKb paling tinggi yaitu 9,38. dimana hal itu menunjukkan bahwa struktur tersebut lebih bersifat asam
1. basa lemah memiliki asam konjugat yang lebih kuat, senyawa yang konjugatnya ... Untuk asam asetat pKa adalah 4,76 (asam kuat) dan untuk etanol pKa adalah 15,9 (asam lebih lemah) ... atom dengan muatan lebih besar memiliki insentif lebih tinggi untuk menstabilkan muatan ini dengan berbagi sepasang ... seperti oksigen dan nitrogen, efek elektronegativitas mendominasi.
BalasHapus